
经济观察网 记者 瞿依贤 6月21日,国家药监局发布《2020年度药品审评报告》(以下简称《报告》),药审中心审评通过20个品种的创新药新药上市申请,审评通过72个品种(含新增适应症品种)的境外生产原研药品新药上市申请。
此外,2020年药审中心审评通过批准临床试验申请1435件,较2019年增长54.97%;审评通过新药上市申请208件,较2019年增长26.83%;审评通过仿制药上市申请918件;审评通过批准一致性评价申请577件,较2019年增长121.92%。
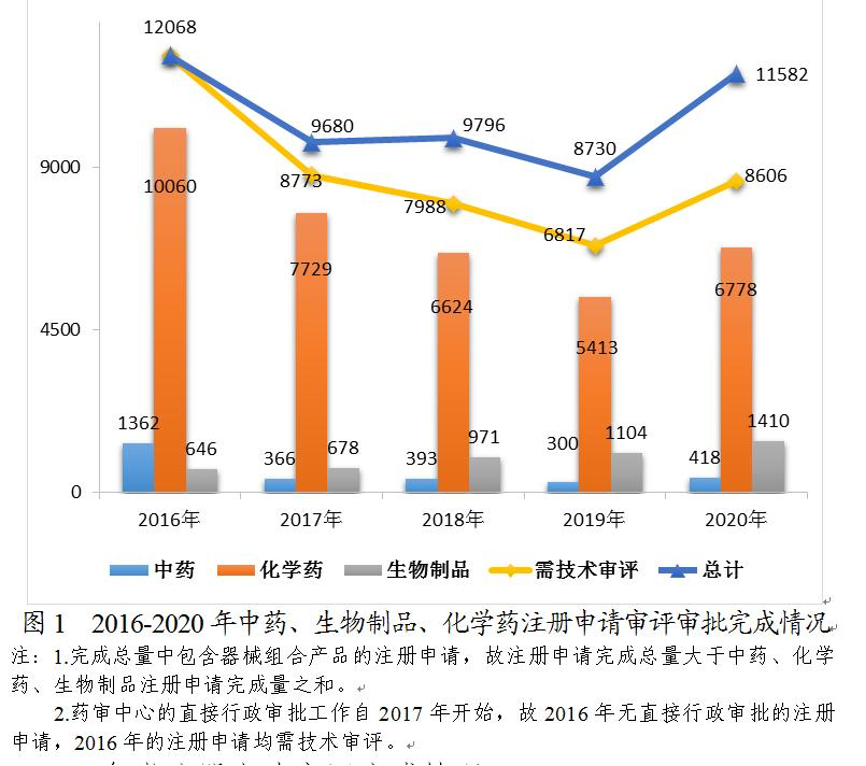
从整体情况来看,去年药审中心完成中药(包括民族药)、化学药、生物制品各类注册申请审评审批共11582件(含器械组合产品4件,以受理号计),较2019年增长32.67%。其中,完成需技术审评的注册申请8606件(含5674件需药审中心技术审评和行政审批注册申请),较2019年增长26.24%;完成直接行政审批(无需技术审评)的注册申请2972件。
在完成8606件需技术审评的药品注册申请中,化学药注册申请为6778件,较2019年增长25.22%;中药注册申请418件,较2019年增长39.33%;生物制品注册申请1410件,较2019年增长27.72%;化学药注册申请约占全部技术审评完成量的78.76%。
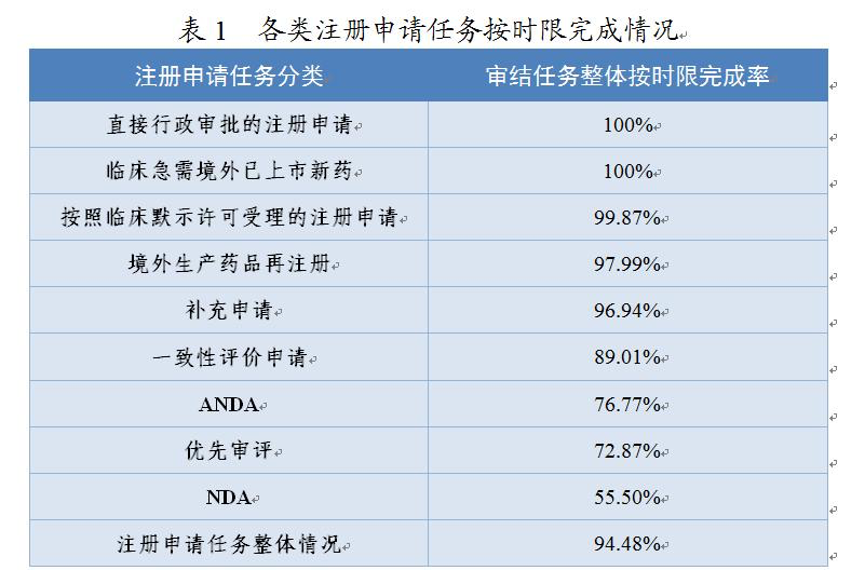
根据《报告》,2020年全年,药审中心审结注册申请任务整体按时限完成率为94.48%,其中临床急需境外已上市新药注册申请审结任务整体按时限完成率为100%,按默示许可受理注册申请的审结任务整体按时限完成率为99.87%,直接行政审批的注册申请100%在法定的20个工作日内完成,且审批平均用时11.8个工作日。
根据《报告》,2020年底正在审评审批和等待审评审批的注册申请已由2015年9月高峰时的近22000件降至4882件(不含完成技术审评因申报资料缺陷等待申请人回复补充资料的注册申请)。

 京公网安备 11010802028547号
京公网安备 11010802028547号