
图片来源:IC photo
经济观察网 记者 瞿依贤 9月6日,国家药监局发布了《2022年度药品审评报告》(以下简称《审评报告》),《审评报告》显示,2022年审评通过建议批准创新药21个,其中3个为首创新药(First-in-Class)——多格列艾汀片、奥木替韦单抗注射液、佩索利单抗注射液;儿童用药批准数量为66个,创历史新高;10个中药新药(包含中药提取物)获批上市;全年整体按审评时限审结率提升至99.80%。
具体到创新药的注册申请受理情况,国家药监局2022年共受理创新药注册申请1794件(1010个品种),同比减少4.88%。
其中,以药品类型统计,创新中药49件(46个品种),同比减少9.26%;创新化学药品1075件(481个品种),同比减少7.80%;创新生物制品670件(483个品种),同比增加0.60%。
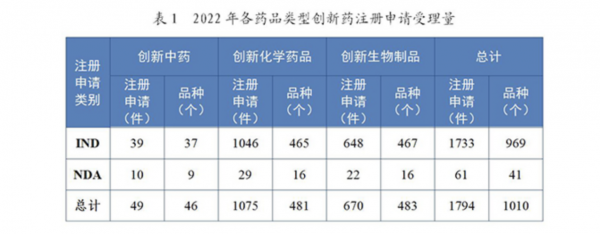
以注册申请类别统计,创新药IND(临床试验申请)共1733件(969个品种),同比减少4.83%;创新药NDA(新药上市申请)共61件(41个品种),同比减少6.15%。

以生产场地类别统计,境内生产创新药1432件(817个品种),境外生产创新药362件(193个品种)。

根据《审评报告》,已发布的三批81个临床急需境外新药中,截至2022年底,已有54个品种提出注册申请,均已获批上市,按时限审结率达100%。
2022年,国家药监局持续加大指导原则制修订力度,发布指导原则61个;推进流程导向科学管理体系建设,将科学管理体系制度文件融入日常审评全流程;加强人才队伍建设,大力支持药品长三角分中心和药品大湾区分中心发展。
国家药监局表示,在2022年世界卫生组织(WHO)疫苗国家监管体系(NRA)评估中,药品注册和上市许可板块获得WHO满分100分和最高评级4级,标志着中国药品审评机构已步入国际先进行列。


京公网安备 11010802028547号